Sigma验证的必要性--从单次检测特性去认识和思考
一、紧紧抓住临床实验室的最突出表现,认识临床实验室开展质量控制的误差概念和建立总允许误差的重要性
走遍世界,不论你在世界的任何一个地方,凡是有临床实验室,收取患者样品,进行医生指定的检测项目(分析物)检测的,均只做一次就发出报告的!50多年前我进入临床实验室,我发现实验室的检测质量很差,是什么原因造成的,让我思考了很长时间!1969年突然让我注意到:只对样品做一次检测,就发出报告,这一定是临床实验室检测结果质量的严重问题。从此,我对临床实验室质量的关注,一切问题的认识和考虑,均从“单次”检测上出发。
实验室的单次检测结果,在数理统计上,它只是一个抽样值!它不是均值!平时,我们希望结果做得好一些,总是说,多做几遍,取一个均值。为什么?因为均值是消除了各个抽样值的随机误差!当然要好得多。当临床对我们的检测结果认为有问题时,要求我们再做一遍。如果与上次检测值很接近,临床医生和患者都认为,上一次结果很准。其实,两次一样,只说明了重复性好,与准确度无关!所以,临床实验室的第一件大事,要千方百计、尽一切可能,确保重复性一定要好!只要精密度好,临床和患者就满意了。
这次,在临床检验医学(Clinics in Laboratory Medicine)杂志上,由Dr Westgard父子俩主编的这期“风险、误差和不确定度:在计量学年代里的实验室质量管理”中,我发现Dr Westgard说了多遍“单次检测”。这是以往Westgard写的文章和演讲内容极少见到的。为什么?由于近期以欧洲检验界和ISO 17511、15189等,规定以不确定度来度量检测结果不可靠性。不断掀起浪潮,要取消Westgard多年来形成的误差概念,要以不确定度来取代误差。
尽管,我知道,早在上世纪70年代时,Westgard在临床实验室完全了解实验室的这个致命问题,才提出了误差理论,提出适合临床实验室的Westgard多规则,并且在世界上提出以总误差(TEa)为临床实验室质量控制的目标。几十年的实践,证明Westgard的总误差理论完全适合临床实验室的实践。所有这些,都是对临床实验室“单次检测”的做法引出的,只是Westgard没有强调。
1、复习单次检测对误差估计的特点
任何检测结果都有误差,因此我们常说结果会不可靠。可是“单次检测”的结果,里面既有随机误差,也有系统误差。我们是如何进行估计的?一个样品只做一次就发出报告,我们确实无法真切了解误差的大小。但是,临床实验室很聪明。我们可以对一个样品特地多做几次,求均值和标准差。对一个仅做一次报告结果来说,若能多做几次后取得的均值,是该样品最可靠的结果,因此一切讨论以均值为中心。标准差是所有各个检测值对于均值的离散程度指标。
因此,临床实验室对自己的行业“单次检测”做法,进行误差估计时:以均值与靶值间有一定方向和大小的差异,称之系统误差(SE),也被称为偏移(Bias)。
所有单次检测结果对于均值的离散,因各个检测值呈随机分布,所以每次检测值对于均值差异的大小为随机变异。为了比较方便,以95%的可能性出现离开均值最大的检测值,它与均值检测差异确定为该检测系统对这个样品检测的随机误差(RE=1.96s)。
若SE与RE的加成在允许误差范围之内,那么该检测系统在该浓度下具有的总误差水平,在可接受低水平。
我希望检验同道不要忘记这样一个做法,我们只是对可能具有的误差进行了估计!一个检测结果内既有系统误差,也有随机误差,以总误差(TE)表示单次检测在均值浓度下具有的误差估计。写作:TE=SE+RE=Bias+2s
2、允许误差(分析质量指标)的共识
1999年4月斯德哥尔摩会议发表的协同声明,是过去16年来临床实验室建立和评估分析质量指标分级的指导原则。这个国际会议是国际临床化学和检验医学联合会(the International Federation of Clinical Chemistry and Laboratory Medicine,IFCC)、国际理论和应用化学联合会(the International Union of Pure and Applied Chemistry,IUPAC)和世界卫生组织(World Health Organization,WHO)组织召开的。
在1999年斯德哥尔摩会议上,Westgard应邀做了“现代质量管理需要一个质量标准的体系”的报告。在报告中,Westgard根据多年来对临床实验室分析质量指标的研究和实际使用情况提出了一个质量标准体系。临床实验室分析质量管理依赖于对检测方法不精密度(精密度)和不准确度(正确度)的评价,并应用统计质量控制程序检出发生在常规分析中的重要的分析误差。Westgard建议在一个质量标准体系中包含不同类型的质量要求,如临床后果指标。从实用角度考虑,所有质量标准均需转换为包含不精密度、不准确度、控制规则和控制检测次数的标准操作规范,而标准操作规范是确保常规检测的分析质量所必须的。
1999年斯德哥尔摩会议,倡导临床实验室分析性能质量指标,应普遍应用等级类别结构对分析性能进行评价。该等级类别具有五个水平:
(1)、评价在特定临床场合下分析性能对临床后果的影响;
(2)、评价分析性能对临床决定的影响,通常使用a)依据生物变异的组分,或b)临床医生观点的分析;
(3)、发表的专业建议,来自a)国家和国际专家团体的,或b)当地专家组或个人的;
(4)、性能目标由a)监督机构、或b)室间质量评估(EQA)计划组织者设定的;
(5)、依据近期操作水平设定的目标,a)由EQA或能力比对试验计划数据展示的,或b)在近期发表的分析发现的。
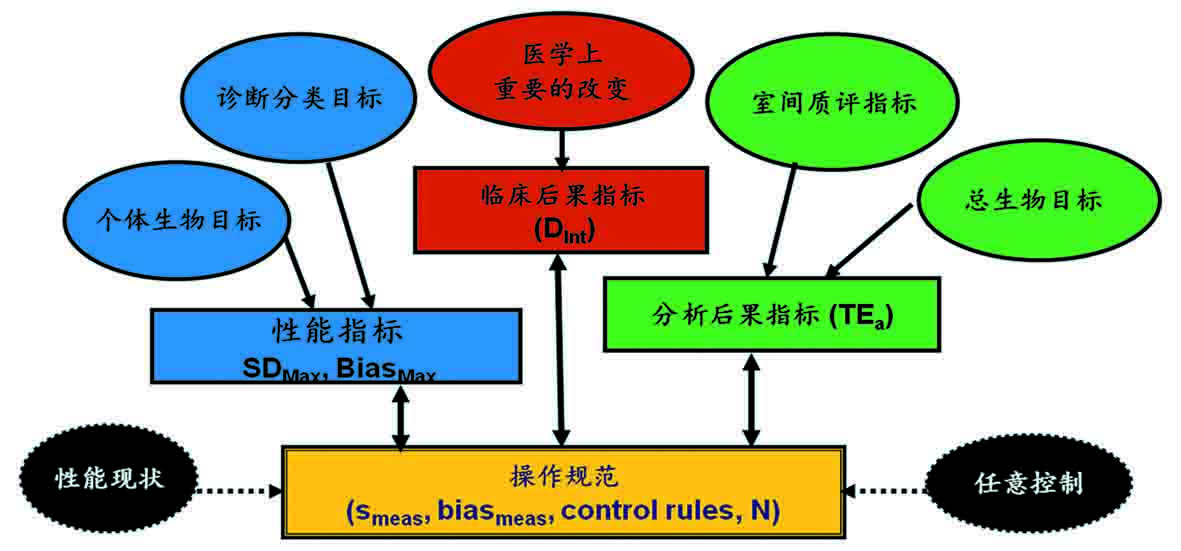
图1、Westgard不同类型的质量指标建议以及它们与不精密度、
不准确度和常规检测需要的质量控制间的关系
二、实验室开展检验必须依赖检测系统;开展质量控制实际是对检测系统质量的控制
1、什么是质量控制?
按照传统的概念,将控制品插在患者样品中,被检测系统检测得到的控制品,绘制在控制图上。从图上观察和了解检测结果是否在控,这是质量控制。不少同事认为做了QC就意味着,我们有了质量。
必须清楚:质量控制是控制质量,不是创造质量!可惜至今有很多的临床实验室,每天在做质量控制,可是究竟在控制什么质量的问题上,没有弄清楚,他们在控制什么质量。
2、需要强化检测系统概念
完成一个患者样品的检测,必须使用仪器、试剂、校准品和操作程序组成的检测系统。保持检测系统完整地长久不变是确保检验质量的重要关键!可惜至今,有太多的实验室一直在自行组合检测系统。仪器是固定的,但使用的试剂常换!尽管使用的校准品是试剂厂商提供的,但是,绝大多数的校准品都不是试剂厂商自行对校准品定值的,是采用了国家药检办同意的罗氏和Randox校准品!这样组合的检测系统,难以确保检测结果的稳定和可靠。
没有检测系统的完整和固定,无法实现临床实验室检测结果的质量。很多实验室认为,试剂厂商的说明书上具有的分析性能是试剂的,这个认识是错误的。完成检验的是仪器与试剂的组合,因此分析性能是仪器与试剂共有的。试剂厂商应该告知:说明书上的分析性能,是在什么仪器和型号上建立的?
3、检测系统分析性能的验证或确认
如果实验室使用了完整检测系统的产品,说明书上指示的分析性能指标是公司的声明,不是你实验室自己的,你必须对声明的性能进行验证,证实在你实验室内,确实具有与厂商声明相同的分析性能。你还必须与你选择的该项目的质量指标(ATE或TEa)比较,证实均在可接受范围内,你方可以有信心进行患者样品的检测。
如果使用的检测系统是你实验室自行组合的,那么在使用该检测系统检测患者样品前,你必须去确认(建立)这个组合的检测系统的分析性能。确认分析性能是一个很复杂的过程。确认分析性能完成后,也就是你已经具有了自己检测系统的分析性能,经过与你选择的允许误差指标(ATE或TEa)比较,均在可接受范围之内,你可以放心地去检测患者样品。
以往对这样的一个分析性能验证或确认过程,只是有实验、有比较;但是不严密,与现在怎样的控制方法没有联系。因此,只认为只要做了质量控制,实验室的质量就可以实现了。是这样吗?
4、质量控制大有文章
目前,开展了每天质量控制的实验室不少,都说是Westgard多规则。但有的实验室认为使用那么多的规则太烦心,就选几个用用就可以了。已经有同事问我,这样可行吗?现在我理解了:尽管每个检测分析物的检测系统被验证可以使用,但是,每个分析物的检测分析性能具有的误差水平不同,与允许误差相比还有多少“余额”也不同。因此,要保持每个分析物的质量,与之配套的控制方法是不同的。近期,Dr Westgard和Sten Westgard已经多年致力于使用Sigma度量每个检测系统的质量水平,去选择最合适的控制方法,非常有价值。
三、Westgard Sigma验证程序的意义
1、Westgard Sigma验证程序的含义:
(1)、临床实验室内使用的检测系统,是否真的符合了验证要求,应采用Sigma度量方式给予验证。
(2)、未被Westgard Sigma验证程序验证过关的,临床实验室必须重新选择其他的检测系统、或努力改善现有的检测系统的质量。直至被验证后,方可检测患者样品。
(3)、对于被验证的检测系统,如果需要通过质量控制保持每次检测具有的质量水平,如该程序验证的水平,则应该按照验证指出该检测系统现有的Sigma度量水平下,去寻找与之合适的控制方法。
仅仅在Westgard多规则中挑选13S、22S、R4S等规则,去进行每天质量控制。以为检测系统分析性能已经被验证、QC也做了,质量没有问题的想法是错误的。
就像一个糖尿病患者,他已经在吃药、定期接受空腹血糖检测、也进行了HbA1C的检查。平时也有些体育锻炼、也注意了饮食控制。可是,每次门诊的空腹血糖依然偏高,在8~9 mmol/L,HbA1C在7.2 %。他自己糊涂了,怎么我的糖尿病这么难治?其实,治疗糖尿病的几个要点,他都没有认真对待,不是吃了药就可以使血糖控制达标的!应该密切注意自己一天之内从晨空腹、早餐后2小时、午餐前血糖、午餐后2小时、晚餐前血糖、晚餐后2小时血糖的表现。应连续有至少有3天的数据,方可提供给临床医生参考,依据这些信息医生可以为患者调整药物的种类和计量。每天锻炼只是意思意思,饭后慢慢走,约20分钟就结束了。他不知道,像我这样的老年患者,每天必须快步走10公里。速度为每分钟120步,锻炼后有点出汗,方才有意义!吃饭没有注意一天的粮食纳入总量,注意一天粮食不应超过5两,要戒酒戒烟!一定要保持HbA1C的水平≤6.0%!只有密切关心与糖尿病关联的每一个方面,认真重视,而且在努力实施的,才会对糖尿病的改善和控制有实际意义!
因此,我希望临床实验室一定要重视:
(1)、做好每个分析物或检验项目的检测系统分析性能的验证!
(2)、依据验证最后总结的,以不精密度和不准确度之和,与允许误差仪器计算的Sigma度量值,作为寻找合适QC方法的方向。
(3)、如实开展QC,不偷懒,认真实施。只有这样,你的质量控制才有意义!
2、Sigma对质量控制要求的度量
使用Sigma度量的做法是:在总允许误差(TAE或TEa)要求下,确定某个分析物临界浓度下的天间不精密度水平(s或CV)。可使用天间重复实验;或控制品的浓度符合要求下,多月的控制图上的CV水平(随机误差水平)。以方法学比较实验,确定该分析物临界浓度下具有的偏移(系统误差水平)。
计算Sigma值:
(1)Sigma≥6选择的控制方法
Sigma值≥6的,为世界级,说明该检测系统分析性能非常优秀。只要求13S控制规则。图中:N=2、R=1(在虚线旁)说明,在单批运行中(R=1),检测两个水平的控制品(N=2)即可(见图2)。
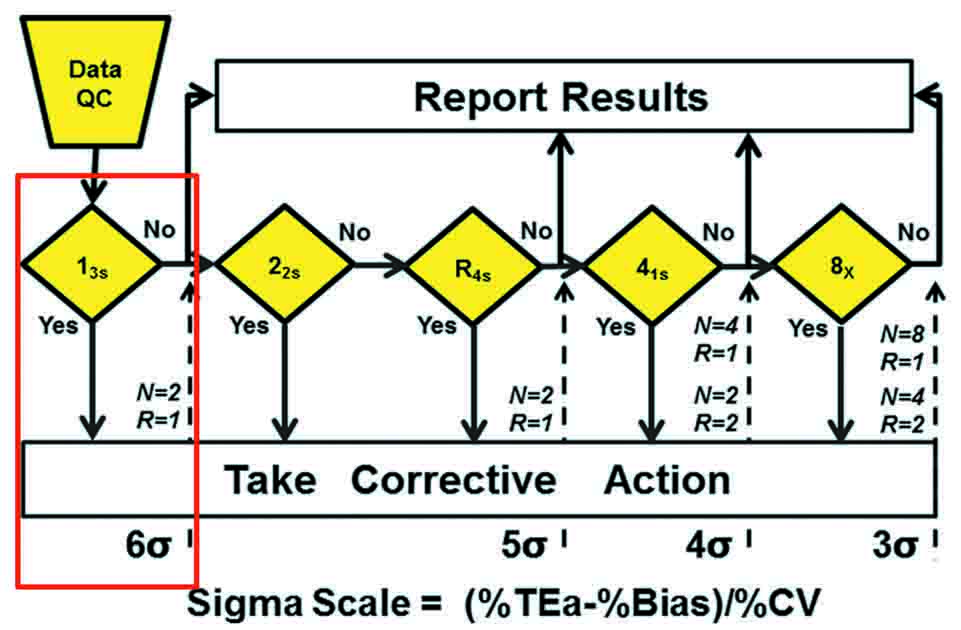
图2、Sigma≥6的多规则示意图(Sigma≥6时,实验室只要在图中红色所示进行控制)。
(2)5 sigma Westgard控制方法
5-Sigma质量要求三个规则:13S/22S/R4S每批检测2个水平控制品(N=2,R=1)。参见下图胆固醇示例。胆固醇5.0 sigma方法。TEa为10%,Bias为0.0%;CV为2.0%。相应的SQC程序是13S/22S/R4S多规则程序。
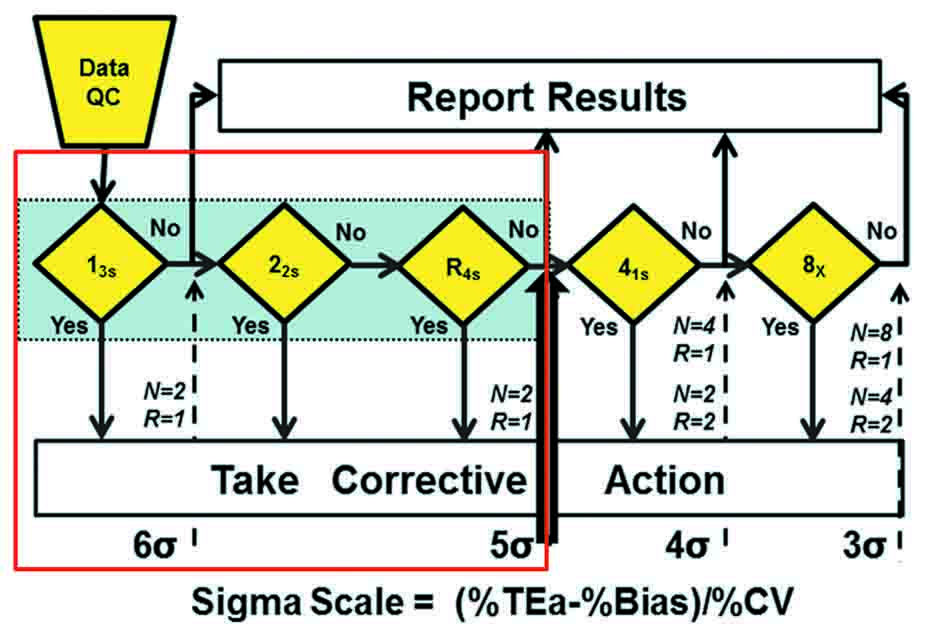
图3、当Sigma≥5的多规则示意图(Sigma≥5时,实验室需要在图中红色所示进行控制)。
(3)Sigma≥4选择的控制方法
4-Sigma质量,要求添加第四个规则,实施一个13S/22S/R4S/41S的多规则。每批最好检测4个控制品(N=4,R=1),或每天分为2批,每批检测2个控制品(N=2,R=2)。
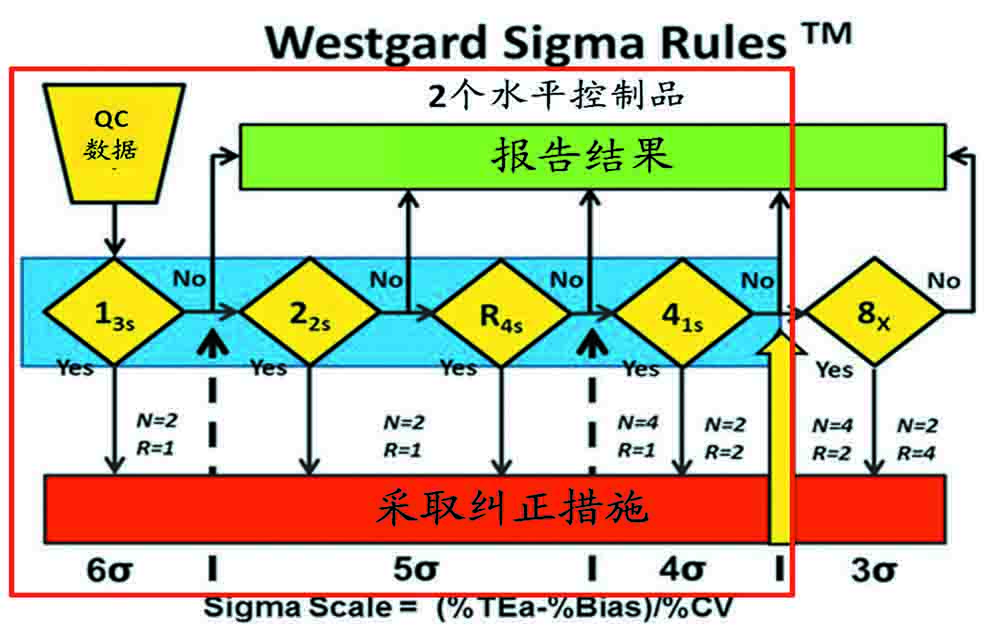
图4、Sigma≥4的多规则示意图(Sigma≥5时,实验室需要在图中红色所示进行控制)。
(4)Sigma<4选择的控制方法
Sigma<4质量的,要求多规则程序,包括8x规则;实施时:将每天工作分为2批,每批检测4个水平控制品;也可将每天分为4批,每批检测2个水平控制品。
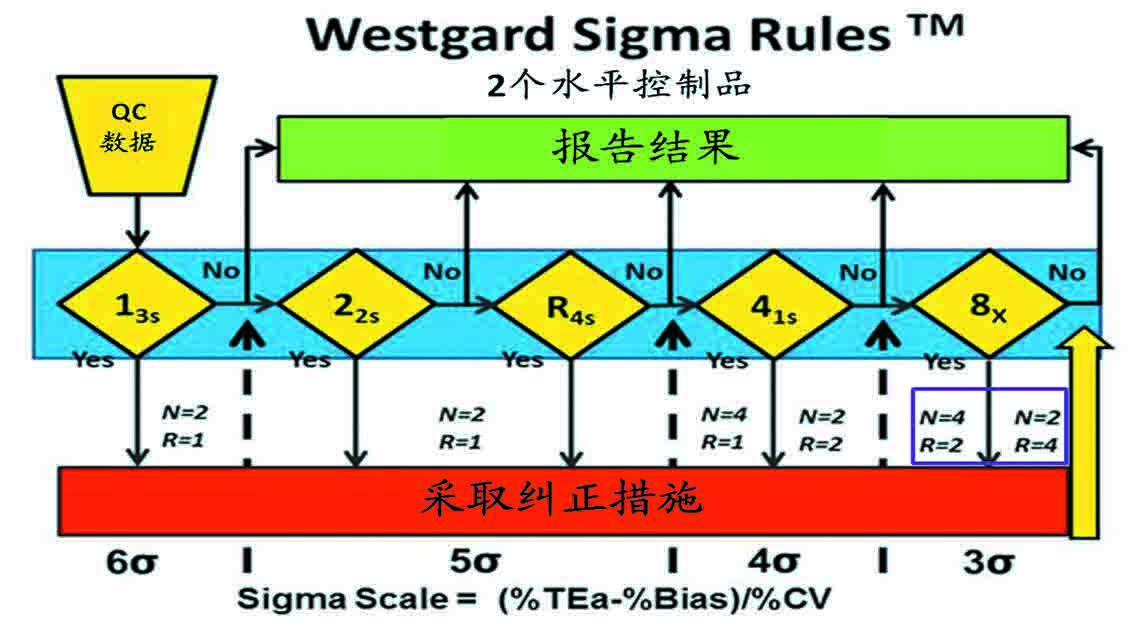
图5、Sigma<4的多规则示意图。
四、总的QC计划
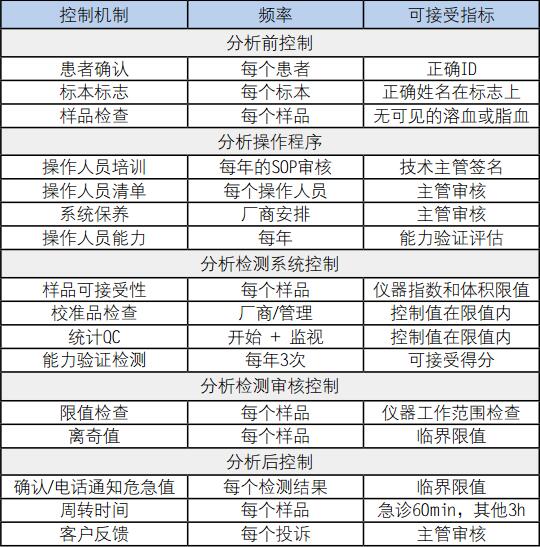
这次,在Westgard新发表的文章中,除了以上使用Westgard的Sigma控制方法之外,还加上以下在风险评估中总结的一些问题(见表),形成实验室的总QC计划。这也可以视为Westgard结合了分析前的风险评估的措施,形成了现今符合美国潮流的风险评估质量控制方法。
表. 总的QC计划示例,证实了控制机制、
使用频率、和可接受性指标
五、关于正确大小的QC计划
在Westgard的文章中,尽管在文章的题目上写出了“正确大小”的QC计划。但是,在文章中似乎没有提及。我的体会是,只要认真重视上述提及的开展质量控制的各个环节,认真努力实施,对于Sigma值小于3的检测系统,不考虑如何配合QC,实验室必须将该系统予以置换外,那么,实验室还是可以完全按照Westgard的Sigma开展方法去实施,不应产生在两个控制间隔间,有患者样品不符要求的问题!
但是,如果实验室根本不顾检测系统的性能如何,只图节约,少做控制,却还追求控制的完美,那么及时在控制规则表现在控下,无法确保患者样品的真实质量。
今年年初,伯乐公司在上海年会前夕推出Parvin理念,对尽管在控的过程中,包含的患者样品不一定都符合质量要求,会有风险的危害。Parvin提出了一个专利的计算方式,可以对任何控制规则、任何控制长度,去估计可能出现患者结果有问题的风险大小。
可是按照Westgard的认识,关键是进行质量控制的程序,必须以Sigma方式进行管理;而且,在实施时,必须到位!只有这样,实验室不必担忧,尽管QC在控,患者结果依然可以确保检测质量。关于这些内容,本人还需认真学习!
六、什么是不确定度?它与误差概念由什么区别?临床实验室为什么无法使用不确定度?
1、2014年的EFLM会议
经历了斯德哥尔摩会议以后15年的不断努力和实践,2014年欧洲临床化学和检验医学联合会(EFLM)在意大利米兰召开了第二次国际会议,期望重新确定分析性能质量。会议对斯德哥尔摩会议的声明进行了重新审核,对原先确定的五个等级建立分析质量指标做法,简化为三个等级,而且还提出了其他的提议。
从一般人眼里,似乎这没有什么大问题。但是,结合这15年以来,对于临床检验的检测结果如何表达结果的质量上,出现了以不确定度替代误差、全面否认了Westgard在临床实验室中为控制误差进行的大量研究和实践。Westgard在许多场合下讲了很多话,也写了很多的文章,这次是一个集中表现。
万万没有想到,2004年引入了ISO 17511的溯源性概念时,根本没有注意文件在讲述溯源性的同时,不确定度概念已经随着文件进入了临床实验室。在推广应用ISO 15189中,申报要求接受认可的临床实验室,必须在检测项目的操作规程中,列出该项目检测的不确定度。为了应对这个挑战,我埋头学习,知道了不确定度的含义和适用性。
2、说说计量实验室参考方法的特点
在计量参考实验室,当实验人员千辛万苦终于对某物质内含有的分析物含量确定了量值后,出具了报告。很快,就有科学家指出,这个值准不准的异议。即如果实验室重新再做一次实验,是否还是今天报告的结果?
要知道,计量参考实验室与我们临床实验室不同的地方,就是(1)他们报告的结果是无数次重复检测后得出的均值;(2)检测的方法已经消除了所有已知的系统误差,即偏移。因此,无数次重复检测还剩下的误差就是随机误差了。
提出不确定度的专家指出:我们无法说出一个检测结果内具有多少随机误差和系统误差。因此,还是对于检测结果的量值而言,有多少不确定性,即不确定度,此话很有道理。但是,这些可以用不确定度描述的结果,均是参考实验室在最佳检测条件下,对一个样品进行了许多(无限)次的检测后的均值,作为该样品的报告值。此时,该报告值依然还有不可靠的可能性。统计上对这样结果量值上的可能性范围,完全可以使用样本均数标准误来估计,这就是经典的不确定度。因此,不确定度只能用于类似临床实验室使用的参考物质,在参考实验室为之定值后,对该定值附加的不可靠性,就是不确定度。
3、回顾临床实验室的误差估计
临床实验室只对患者标本检测一次的结果,只是一个检测的抽样值,它根本不是均值。没有资格采用诸如样本均值标准误来对它结果检测值进行所谓量值不可靠性的估计,即总体均值的可信范围。
不确定度本来是参考实验室对使用严密的参考方法对样品检测结果可靠性的估计(至少是许多次、甚至是无限多次的检测;而且在检测前,对出现的偏移,事先都进行了纠正,也即检测方法一定是无偏移的方法)。
但今天临床实验室的检测方法或检测系统间不具有可比性的,照样在使用检测,哪里有去除偏移的可能性!
4、要求临床实验室应用的不确定度
由于IFCC在GUM上签字,承诺在临床实验室使用不确定度,才出现了今天的争论!但是面临的问题许多:
(1)、一个检测结果必须与一个不确定度与之对应。临床实验室每天发出的检测结果成千上万,实验室该如何配合计算每个检测结果的不确定度呢?
(2)、不同检测浓度下的不确定度完全不同。如何对报告结果浓度分布很宽的情况下,报告不确定度?
因此,今天在ISO 15189上的要求,变成:一个实验室的一个分析物的所有检测结果,只要采用日常QC的较长周期的CV,乘2即2CV就是该分析物在该实验室的结果不确定度!不确定度的严密科学性何在?
5、Westgard的苦恼!
他是全世界的知名专家,他为临床实验室的质量管理做了许多工作。今天的分析质量误差估计等的做法,都是他建立和使用的。而今天追求溯源性和不确定度的,一心要全世界的临床实验室领域,成为不确定度的天下!这是从1993年提出体外诊断产品导则开始,一步步走来的,先是提倡检测结果需要溯源性。可是,当时大家还没有彻底思考清楚时,都说有道理。一时间有无溯源性成为一个产品、一个检测结果有无质量的“标志”!
紧接着,不确定度跟着溯源性,出现在我们国内。一些国内知名人士一起追捧,变得临床实验室一定要用不确定度。我就在这样的情况下,去学习不确定度的。我的观点与那些认可ISO 15189和要实施不确定度的大家不同,很快我就变成众矢之的。可惜,我的存在不拜倒在别人的脚下!别人说什么,任他说去!我做我喜欢的。所有一切都必须要实事求是!Westgard已经世界闻名,要在国际上树立一切由不确定度概念领导,非要将Westgard的误差理论打下去,Westgard太苦恼了!
Westgard一边要应付那么多奇谈怪论,一边还在想:不确定度那么想钻进临床实验室质量管理领域,为什么我们的临床实验室误差理论不可反过来,去迫使计量测量专家不得不承认误差理论和概念?现在,临床实验室已经在使用不确定度上,计量专家已经大大退步;面临对检测(测量)方法一定要去除偏移才可使用的观点!这是不确定度以2CV表达的依据;但在临床实验室根本无法去除,大量检测方法间有明显的偏移,都在使用的现实,实在棘手!
如果要临床实验室将不确定度用起来,看来不承认在不确定度内没有偏移是太困难了。现在,就是在考虑如何承认这个偏移的“不确定度”!
如果计量学上不确定度观点,一旦承认将偏移也作为不确定度予以考虑的话,那么,不确定度理论在临床实验室的实践面前全面崩溃!到时,临床实验室也无所谓误差理论或不确定度理论,也许到那时候,不确定度的含义都已经发生了完全的变化。正如一些专家认为的,未来是否将误差理论与不确定度结合起来?当然,误差和不确定度双方正在理论上苦战!感谢Westgard!
七、总结
我永远坚持以“临床实验室一直只对样品做一次检测就发出报告”,作为我们必须开展质量控制的出发点!
临床实验室做检测的第一个要做好的就是重复性!没有良好精密度的结果,毫无价值!即使有可溯源的依据,结果没有意义!因此,我们临床实验室根本不是可以使用不确定度的地方,只有参考实验室有资格。如果你认为我们必须应用不确定度,那么请看看这次Sten Westgard的文章!他如实的调查,说明世界上所有临床实验室,都没有不确定度的站脚点!ISO 15189的要求不实事求是!
2017年刚刚开始,我们已经投入了紧张的工作。临床实验室实在是很小很小的一个专业部门,但是它担负着人的生命和健康的重担!我真的感到,需要去理解和学习的内容太多,我有点来不及。但是,我相信只要去学习!
可是,在任何时候,我们都不要忘记,我们所在的国家!她在不断地发展和变化!老百姓需要得到基本的健康保障!我们有责任去尽力做好它!与大家共勉!
参考文献
1、James O.Westgard,Sten A.Westgard. Measuring analytical quality. Total analytical error versus measurement uncertainty. Clin Lab Med 2017; 37(1):1-13.
2、Sten A.Westgard. Rhetoric versus reality ? Laboratory survey show actual practice differs considerably from proposed models and mandated calculations. Clin Lab Med 2017;37(1):35-46.
3、James O.Westgard, Sten A. Westgard. Six sigma quality management system and design of risk-based statistical quality control. Clin Lab Med 2017; 37(1):85-96.
4、David Armbruster. Mtrological traceability of assays and comparability of patient test results. Clin Lab Med 2017;37(1):119-135.
5、James O.Westgard. A total quality-control plan with right-sized statistical quality-control. Clin Lab Med 2017; 37(1):137-150.




