癌胚抗原检测试剂盒(磁微粒化学发光法) 的性能评估
癌胚抗原(Carcinoembryonic Antigen,CEA)是由加拿大学者Gold和Freedman于胎儿及结肠癌组织中首先发现的[1]。CEA主要存在于直肠、结肠癌组织和胚胎肠粘膜上,因这种抗原也存在于2-6个月胚胎的胃肠、肝脏和胰腺组织中,故名癌胚抗原。CEA浓度升高与多种肿瘤尤其是消化道肿瘤相关,如结肠癌、直肠癌、胃癌、胰腺癌、胆管癌等,肺、乳腺及泌尿生殖系统的恶性肿瘤也会出现不同程度的升高[2]。其中,结肠癌有较高的阳性率,且阳性率与癌肿组织中CEA的含量呈正相关;同时CEA的含量与肿瘤浸润深度有关。在临床中CEA常与多个肿瘤标志物联合检测,用于肺癌、胃癌、结直肠癌等多种肿瘤的早期诊断、疗效和预后评价[3-5]。
本实验室采用郑州安图生物工程股份有限公司生产的癌胚抗原检测试剂盒(磁微粒化学发光法),评估其分析性能,且与德国罗氏公司电化学发光法试剂进行方法学比对,对其有效性提供了重要依据。
1、材料与方法
1.1 材料
1.1.1 试剂
评价试剂:郑州安图生物工程股份有限公司生产的癌胚抗原检测试剂盒(磁微粒化学发光法);
参比试剂:德国罗氏公司生产的癌胚抗原定量检测试剂盒(电化学发光法)
1.1.2 质控
(1)可报告范围质控血清:选取3份不同浓度的CEA高值样本,用
健康人样本稀释21倍,用于报告范围性能验证;
(2)精密性质控:选取高、低两份样本,用于精密性实验;
(3)准确度参考物质:采用国际标准品WHO 73/601,稀释后用于
准确度实验;
(5)干扰质控品:将血红蛋白、甘油三酯、胆红素分别按照合适
的浓度加入到高、低两份样本中,用于内源性干扰样本;
(6)企业一级校准品:郑州安图生物工程股份有限公司提供。
1.1.3 样本
选择2016年3月至2016年12月由河南省中医院诊治的相关样本共计844例,分别如下:胰腺肿瘤16例,结肠恶性肿瘤32例,直肠恶性肿瘤43例,肺部恶性肿瘤127例,宫颈恶性肿瘤21例,胃部肿瘤121例,肝恶性肿瘤36例,乳腺恶性肿瘤80例,食管恶性肿瘤43例,子宫内膜恶性肿瘤22例,卵巢恶性肿瘤36例,其他147例,体检样本120例,用于方法学比对。
1.1.4 实验仪器
评价试剂配套仪器:AutoLumo A2000系列发光仪(郑州安图科技股份有限公司);
参比试剂配套仪器:Cobas e601(德国罗氏公司)。
1.2 方法:所有考核均依据《体外诊断试剂分析性能评估系列指导原则》,同时参照相关性能的EP文件。
1.2.1 分析灵敏度评估:参考CLSI EP17文件提供的方案,用评价试剂检测重复测定0水平校准品20次,计算分析灵敏度;
1.2.2 线性范围评价:参考CLSI EP-6A文件提供的方案,用评价试剂检测梯度稀释的企业一级校准,评价其线性范围;
1.2.3 可报告范围评价:参考CLSI EP-6A文件提供的方案,用低值样本稀释3个水平的高值样本,稀释倍数为21倍,用评价试剂检测,检测结果回算浓度与高值样本结果比较偏差应小于10%;
1.2.4 准确度评价:参考行业标准,将WHO 73/601稀释至100ng/ml,用评价试剂检测;
1.2.5 精密度评价:参考CLSI EP5-A文件提供的方案,用三批试剂分别考核低、高两份样本,计算分析内、批间变异;
1.2.6 干扰实验;参考CLSI EP7-A文件提供的方案,用高、低两份样本分别稀释血红蛋白、甘油三酯和胆红素,用三批试剂分别检测,与未添加样本平行检测,计算干扰因素前后的百分偏差;
1.3 统计学处理:采用SPSS19.0软件进行统计学分析,采用多项回归分析并计算ADL,当ADL小于相应临界值时认为多项式具有临床可接受的非线性;一致性评价采用Kappa一致性检验,相关性分析采用Pearson相关性分析,线性回归分析采用简单线性回归分析,当P<0.05时表示差异有统计学意义。
2、结 果
2.1 分析灵敏度评价:剂量反应曲线见图1,评价试剂的分析灵敏度水平平均值为0.20ng/ml。
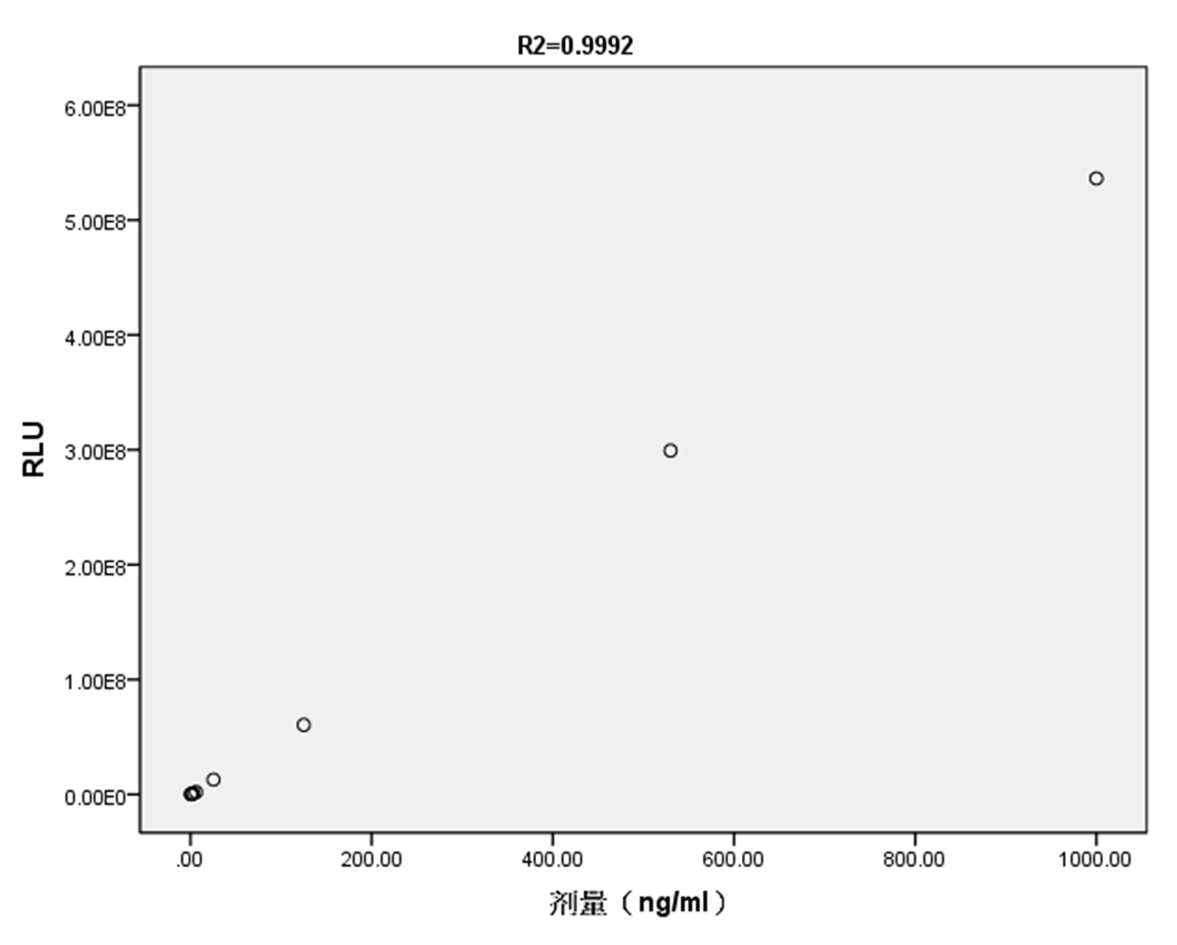
图1. 试剂A(20160218)的剂量反应曲线
2.2 线性范围评价:该试剂盒线性范围为0.5-1000ng/ml。
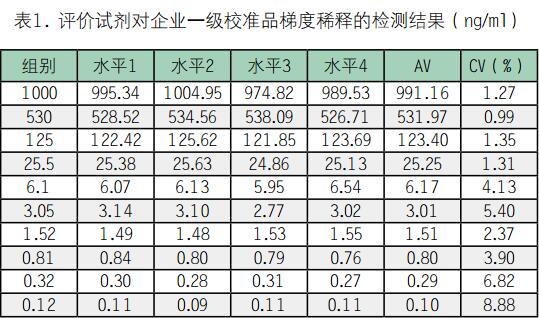
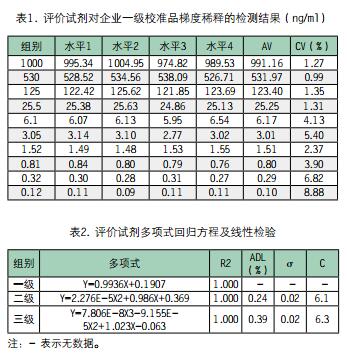
2.3 可报告范围评价:高值标本进行21倍稀释时,测定水平与理论水平的偏差Bias均小于5%,可报告范围下限为0.5ng/ml,上限为 21000ng/ml,因此该试剂盒可报告范围为0.5-21000ng/ml。
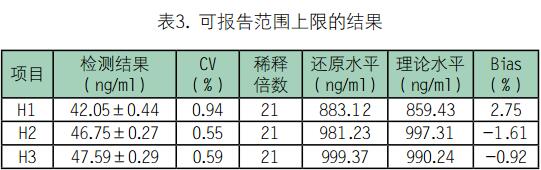
2.4 准确度评价:稀释检测WHO 73/601,准确性为94.21%~106.61%。
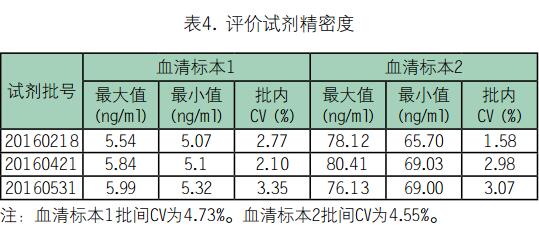
2.5 精密度评价:批内精密度为1.58-3.35%,批间精密度为4.55-4.73%,试剂盒的重复性良好,见表4。
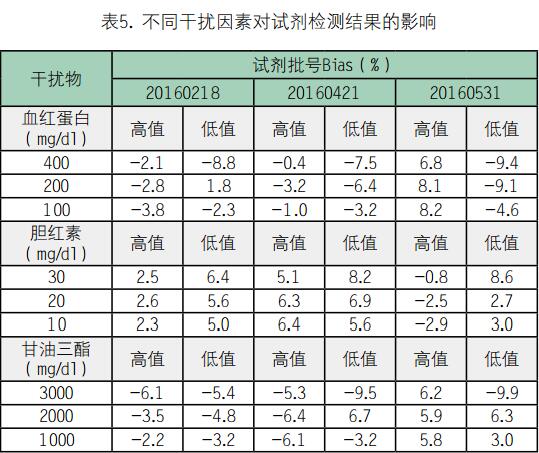
2.6 干扰试验:溶血、胆红素、甘油三酯对评价试剂影响较小,添加干扰因素后的Bias均在10%以内。
2.7 方法学比对试验:评价试剂与参比试剂呈良好的线性关系,线性回归方程为Y=1.0311X+0.4166(R2=0.9902,P<0.05),同时一致性比较及相关性分析的结果显示评价试剂与参比试剂具有良好的一致性(Kappa=0.967,P<0.05)及相关性(r=0.9950,P<0.05),总符合率为99.64%。
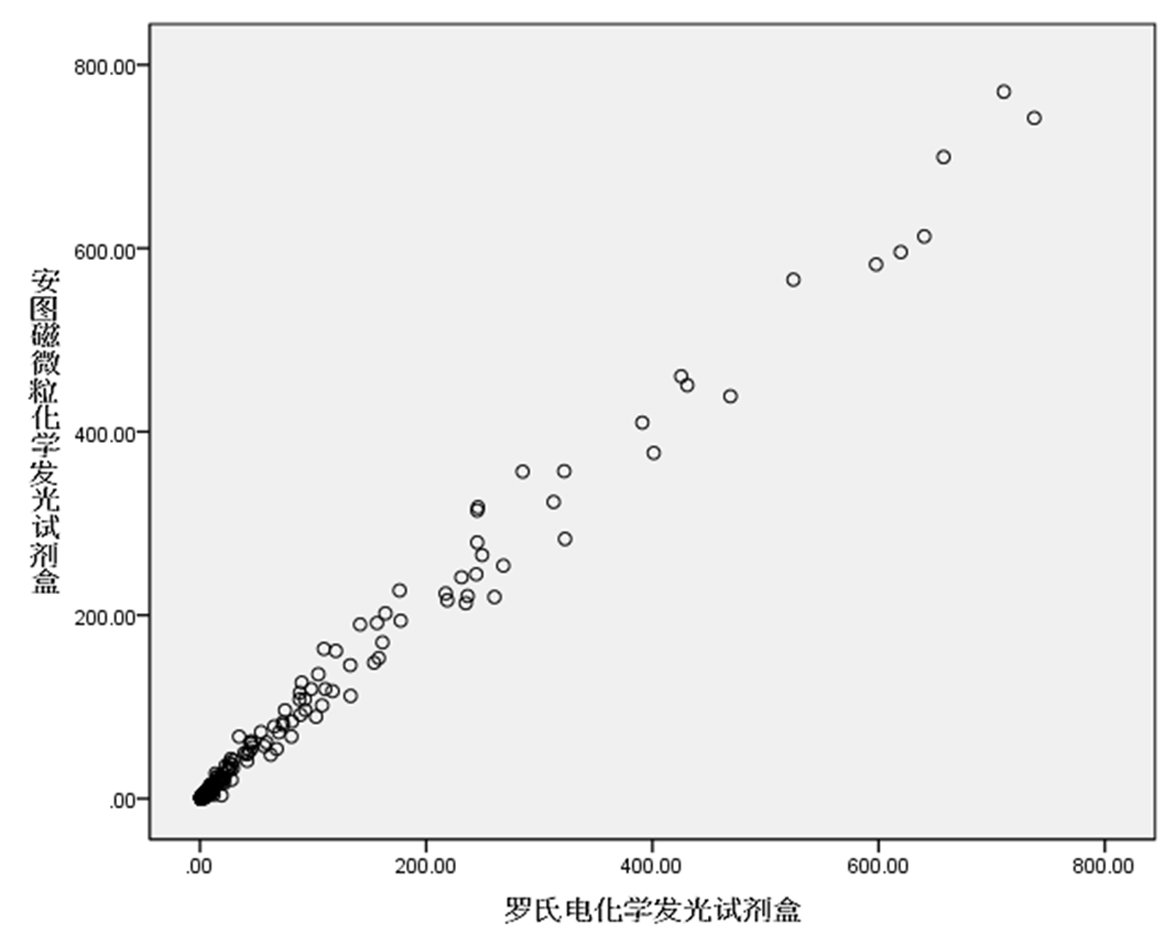
图2. 评价和参比试剂血清 CEA 检测结果线性相关拟合
各类肿瘤中,胰腺肿瘤的阳性率最高(53%),其次是结直肠癌(48%),然后是肺癌(44%)、宫颈(29%)及胃癌(28%),对肝癌(22%)、乳腺恶性肿瘤(19%)和食管恶性肿瘤(7%)均有一定的阳性率。
3、讨 论
CEA的检测方法主要有电化学发光法、磁微粒化学发光法、化学发光法和酶联免疫吸附法,其中电化学发光法和磁微粒化学发光法在灵敏度、特异性和检测线性等方面均有明显的优势。在临床上CEA已作为一项常规的检查项目。
研究显示,3.7%的无症状者在体检时发现CEA水平不明原因的升高[6],建议对患者进行动态监测,血清CEA水平异常升高或进行性升高常提示恶性肿瘤。
本实验室对安图生物工程股份有限公司生产的癌胚抗原检测试剂盒(磁微粒化学方法)的性能进行评估,并与罗氏电化学发光法进行平行比对临床相关和阳性率,结果显示,评价试剂与参比试剂间具有很高的临床一致率,相关性r为0.9950,总符合率为99.64%,一致性较好(P<0.05,Kappa=0.967)。评价试剂的批内和批间精密性优越,具有较高的分析灵敏度,准确度满足行业标准要求,可报告范围及内源性干扰指标均可满足临床检验要求。说明评价试剂与目前临床上广为应用的进口试剂在指标检测性能上具有良好的等效性,可替代国外昂贵试剂应用于临床检测。
郑州安图生物工程股份有限公司 供稿
参考文献:
[1] Gold P, Freedman SO. Demonstration of tumor-specific antigens in human colonic carcinomata by immunological tolerance and absorption techniques[J]. J Exp Med, 1965,121:439-462.
[2]尚高峰,张翠歌。癌胚抗原检测的临床意义[J]。内蒙古中医药,2014,33(33):57-58.
[3] 潘丽兰。血清CEA、CA199、CA125、CA153、AFP联合检测对胃癌的诊断价值[J]。中国实验诊断学,2013,17 (12):2192-2195.
[4] 张海英。癌胚抗原和糖类抗原125联合检测在肺癌诊断中的应用[J]。检验医学与临床,2013,(24):3335- 3336.
[5] 卢灿荣,张士武,张勇等。联合检测癌胚抗原、糖链抗原19-9和C反应蛋白对结肠癌的诊断价值[J]。标记免疫分析与临床,2012,19(1):3-6.
[6] Li WF, Yin WW, Ou RY, et al. The value of F-18 fluorodeoxyglucose positron emission tomography/computed tomography in asymptomatic examinees with unexplained elevated blood carcinoembryonic antigen levels[J]. Eur J Nucl Med Mol Imaging, 2016,43(4):65-681.




